
Hospital Regional Dr. Rafael Henández Loeche, Chiriquí. Panamá
Recibido 20 de agosto 2024; aceptado 10 de septiembre 2024
Disponible en internet el 31 de enero 2025
Palabras Clave: Laparoscopía, Cirugía laparoscópica , Seguridad del paciente.
Key Words: Laparascopy, Laparscopic surgery, Patient safety.
RESUMEN
La cirugía laparoscópica se ha consolidado como el método de elección para la resolución de la mayoría de las patologías quirúrgicas abdominales racias a los multiples beneficios que ofrece tanto al cirujano como al paciente en términos de seguridad y recuperación. El concepto de cirugía mínimamente invasiva se encuentra en constante evolución y expansión, siendo uno de sus principales avances la introducción de cirugía robótica que paulatinamente va adquiriendo un rol protagónico en las especialidades quirúrgicas. El entendimiento de los fundamentos en cirugía laparoscópica general es esencial para adquirir las destrezas requeridas en las modalidades mínimamente invasivas más avanzadas. El presente manuscrito busca recopilar los principios técnicos de la cirugía laparoscópica abdominopélvica.
ABSTRACT
Laparoscopic surgery has been established as the gold standard treatment for most surgical abdominal pathologies due to its multiple benefits or both sur eons and patients in terms o securit and recover . The concept of minimally invasive surgery is constantly evolving and expanding, with one of its major advances being the introduction of robotic surgery which is gradually taking on a leading role among certain surgical specialties. Understanding the basics of general laparoscopic surgery is essential to develop the abilities required for other more advanced modalities. This manuscript seeks to compile the technical principles of abdominopelvic laparoscopic surgery.
INTRODUCCIÓN
Los multiples beneficios documentados con la cirugía mínimamente invasiva en los últimos 120 años han motivado al cirujano a considerar este tipo de abordaje como primera línea para la resolución de diferentes patologías de la cavidad abdominal. (1) La laparoscopía, cuyo origen etimológico viene del griego “laparo” (abdomen) y “scopein” (examinar), se basa en la inserción de una cánula a través de la pared abdominal, distensión de la cavidad con gas y visualización de los contenidos gracias a una cámara iluminada. (2)
La historía de la cirugía mínimamente invasiva tiene su origen en 1901, cuando el Dr. Georg Kelling ingresa a la cavidad peritoneal canina. El primer intento en humanos sería llevado a cabo por Jacobaues en 1910, sin embargo, se vería limitado por la pobre visualización obtenida por los insumos de aquella época. (2)
Gracias a los avances obtenidos en el campo tecnológico durante las décadas de 1960 y 1970, el ginecólogo Kurt Semm reporta la primera apendicectomía laparoscópica en 1983, seguida en 1987 por la publicación de la primera colecistectomía vía técnica laparoscópica, obra de los cirujanos franceses Phillip Mouret y Francois Dubois. (1,2) El doctor Eric Muhe había realizado dicho procedimiento dos años antes, sin embargo, no fue publicado. (1)
Al igual que la modalidad abierta, en la cirugía laparoscópica el aprendizaje se obtiene mediante entrenamiento contínuo, lo cual supone una comprensión adecuada y obligatoria de las técnicas quirúrgicas y el funcionamiento de sus equipos e instrumentos para el cirujano en formación y personal que conforma el equipo quirúrgico.
Los pilares de la cirugía mínimamente invasiva abarcan desde la colocación del paciente, ergonomía transoperatoria insuación de neumoperitoneo para la profilaxis de tromboembolismo venoso. Según dicha publicación, debe valorarse el riesgo según las escala de Caprini (5) o Rogers (6): Riesgo muy bajo (Caprini 0, Rogers menor de 7): deambulación con sus repercusiones hemodinámicas, inserción de trócares, manejo de laparoscopio, técnicas de disección que incluyen el uso de energía quirúrgica especializada y hasta la posible conversión a una modalidad abierta o tradicional, en función de los hallazgos transoperatorios (3).
PREPARACIÓN
Etapa más importante en cualquier procedimiento quirúrgico. Incluye el planeamiento del manejo de hemoderivados según el tipo de cirugía a realizar y protocolos locales. (2)
Transfusión sanguínea (2)
El sangrado es considerado una de las principales complicaciones de la cirugía laparoscópica. Para los procedimientos de alto riesgo de hemorragia (colectomías, resección hepática, esofagectomía), se recomienda el cruce de unidades de glóbulos rojos empacados preoperatoriamente. En el caso de cirugías de bajo riesgo de sangrado (apendicectomía, colecistectomía), la opinión es dividida. El abordaje en estos casos debe realizarse según los protocolos locales, sobre todo en el contexto de procedimientos de urgencia.
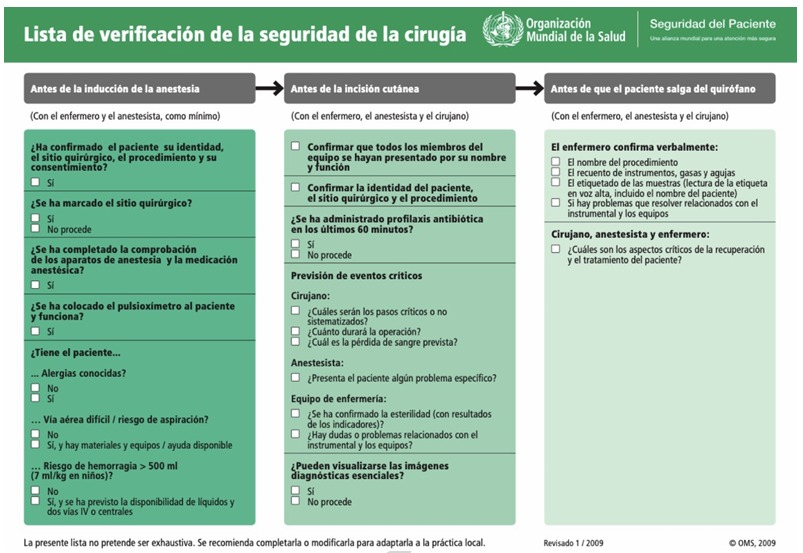
Lista de verificación preoperatoria (2)
Resultados de un estudio llevado a cabo por la Organización Mundial de la Salud (OMS) demostró que la implementación de una lista de verificación de seuridad de la ciru ía fi ura 1 reduce las complicaciones posoperatorias en los primeros 30 días del 11 a 7%, así como la mortalidad del 1.5 a 0.8%.
Tromboprofilaxis (4)
La Sociedad Americana de Cirujanos Gastrointestinales y Endoscopistas (SAGES, por sus siglas en inglés), ha aprobado la utilización de las guías publicadas en el 2012 por el Colegio Americano de Médicos del Tórax (ACCP, por sus siglas en ingles) para la profilaxis de tromboembolismo venoso. Segun dicha publicación, debe valorarse el riesgo según la escala de Caprini (5) o Rogers (6):
Riesgo muy bajo (Caprini 0, Rogers menor de 7): deambulación temprana sin profilaxis farmacológica o mecánica
Riegos bajo Caprini 1-2 Rogers 7-10 profilaxis mecánica (compresión neumática intermitente, CNI).
Riesgo moderado (Caprini 3-4, Rogers >10):
• Sin alto riesgo de sangrado: heparina de bajo peso molecular (HBPM), heparina no fraccionada HN a dosis bajas o profilaxis mecanica CNI .
• Con alto riesgo de sangrado: CNI.
Riesgo alto (Caprini >5):
• Sin alto riesgo de sangrado: HBPM o HNF a dosis bajas adicional a medias elásticas o CNI.
• Con alto riesgo de sangrado: CNI hasta la disminución de dicho riesgo posterior inicio de profilaxis armacológica.

Equipamiento (2,3,5)
Equipo quirúrgico
• Anestesiólogo: la interdependencia con el cirujano radica en la generación de neumoperitoneo y la regulación de sus efectos, los cuales serán abordados en la sección “Acceso inicial a la cavidad abdominal”.
• Personal de enfermería: llevan un registro de la lista de verificación preoperatoria, vigilan el desarrollo adecuado de la intervención, comprueban los parámetros de los equipos los modifican se n la necesidad del cirujano y supervisan el seguimiento de los protocolos de seguridad del quirófano.
Entorno
• Quirófano: debe contar con la iluminación adecuada y una extensión de sus dimensiones que permita la movilización del cirujano sin obstáculos (mínimo una extensión total de aproximadamente 37 m2).
• Mesa de operaciones: la altura de la mesa se ve inuenciada por neumoperitoneo el cual eleva la pared abdominal más o menos 10 cm. Sumado a la extensión de los instrumentos, la altura a alcanzar por el cirujano puede aumentar unos 30cm. Es importante comprobar el funcionamiento de la mesa quirúrgica previo a la cirugía para las lateralizaciones adecuadas según cada procedimiento.
Posicionamiento y ergonomía
Es deber del cirujano principal y sus asistentes asegurar un adecuado posicionamiento del paciente y la ergonomía transoperatoria.
Posicionamiento del cirujano
Se reporta lesiones músculo-esqueléticas en 73 a 100% de cirujanos debido a pobre ergonomía. La posición correcta debe incluir:
1. Hombros relajados con brazos en ligera abducción.
2. Codos e ionados en un ángulo de entre 60 y 90º (en ocasiones es útil posicionarse sobre un estrado o colocar la mesa quirúrgica a su altura más baja).
3. La colocación del monitor de frente al cirujano principal entre 0 y 15º por debajo del nivel de los ojos y la imagen captada por la camara debe tener una posición central. Se recomienda evitar el exceso de monitores para una mejor concentración
4. El pedal de trabajo al mismo nivel que los pies de cirujano y en dirección a objetivo anatómico
Posicionamiento del paciente
La posición se determinará según el área anatómica a abordar, siendo la más ampliamente utilizada el decúbito supino.
Se recomienda para prevención de deslizamientos y neuropatías del paciente:
• Utilización de fundas de silicona y restringidores (en dependencia del procedimiento a realizar).
• Evitar angulaciones de mesa quirúrgica mayores de 30º por el riesgo aumentado de caídas.
• Aducción de miembros superiores (requiere vigilancia de acceso venoso).
• Rotación interna de miembros inferiores (prevención de lesión del nervio peroneo) para obtener alineación de tobillos y rodillas con el hombro contralateral. (2).
Concepto de diamante de béisbol
La ubicación de la óptica y puertos de trabajo principales se simplifican con este principio. Consiste en crear la analogía de considerar el puerto destinado a la óptica como “Home plate”, el objetivo anatómico de la cirugía como “segunda base” y la “primera base” y “segunda base” como primer y segundo puertos de trabajo, respectivamente.
Ejemplos de posicionamiento de paciente comúnmente empleados
• Colecistectomía: decúbito supino con lateralización a la izquierda y anti-Trendelenburg. Cirujano principal y primer asistente a la izquierda del paciente. Monitor de laparoscopia hacia el hombro derecho del paciente.
• Apendicectomía: decúbito supino con lateralización a la izquierda y Trendelenburg, miembros superiores en aducción. Cirujano principal y primer asistente a la izquierda del paciente. Monitor a la derecha del paciente hacia miembros inferiores.
Cabe resaltar que la elección de estas colocaciones va a depender de las características físicas del paciente y del entrenamiento y preferencia del cirujano.
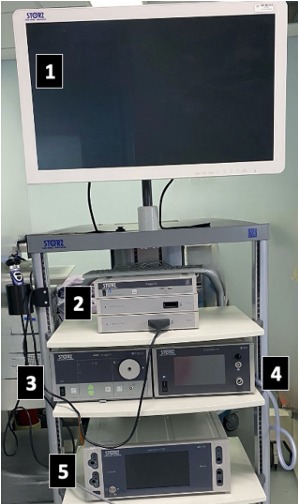
Torre laparoscópica
Los componentes que describiremos a continuación se encuentran generalmente ubicados en el complejo conocido como torre de laparoscopía:
1. Monitor: se coloca en la parte más alta de la torre y está frecuentemente adaptado a un brazo rotatorio para su posicionamiento. Se puede contar con monitores auxiliares externos a la torre según necesidad. Las versiones más recientes presentan tecnología para imágenes de alta resolución.
2. Cámara: consiste en un cabezal que se acopla al laparoscopio rígido. Cuenta con controles de mando para el ajuste de resolución (foco) y apertura de campo visual o diafragma.
3. Fuente de Luz: la luz se genera a partir de una fuente externa y pasa hacia el laparoscopio a través de un cable de fibra óptica. En la actualidad se utilizan fuentes de diodo emisor de lu LED. El extremo distal de esta fibra alcana altas temperaturas y puede producir lesiones térmicas en el paciente o al material quirúrgico.
4. Insuador dispositivo diseado para la introducción de gas en la cavidad. Cuenta con controles para ajustar los parámetros de presión en mmH uo en lmin así como un monitor del uo total administrado. El reservorio de as se conecta al insuador el cual presenta un indicador de cantidad de gas disponible.
5. Energía quirúrgica: consolas para dispositivos diseñados para laparoscopía accionados por energía quirúrgica convencional (monopolar o o bipolar), así como energía ultrasónica combinación de múltiples modalidades.
Instrumentos (4, 5)
Lente rígido o laparoscopio
Sus principales aspectos técnicos son su tamaño (los más utilizados de 10, 5 y 3 mm), y angulación (planos o 0° y biselados de 30°, 45°). Los lentes angulados pueden lograr ángulos de hasta 135º y alcanzar mejor visualización de los extemos de la cavidad.
Trócares o puertos
• Principales aspectos técnicos: diámetros (3mm, 5mm, 10-12mm), longitud (para cirugía convencional, pediátrica, bariátrica), tipo de punta (cortantes y atraumáticos).
• Con frecuencia, el trócar inicial es de 10-12mm, a nivel umbilical y la colocación de los demás se da posterior a la insuación del neumoperitoneo.
• Puertos secundarios: Colocación debe realizarse bajo visión directa para evitar lesiones iatrogénicas, dependerá del tipo de procedimiento y de los hallazgos transoperatorios (adherencias, colecciones). El cirujano debe distinguir entre los trócares de trabajo de los trócares de exposición. Los primeros, deben permitir al instrumento alcanzar el sitio quirúrgico con el máximo de ángulos de abordaje posible. Los trócares de exposición pueden ubicarse lejos del objetivo anatómico para cumplir su función.
• La colocación, cantidad y tamaño de trócares también se decidirá según la necesidad de utilizar equipo adicional. No debe limitarse la colocación de un trócar adicional para brindar mayor seguridad y simplicidad quirúrgica.
• Para minimizar el riesgo de hemorragia durante la inserción de puertos secundarios puede realizarse la transiluminación de la pared abdominal con el laparoscopio. La lesión de la arteria epigástrica inferior es evitable mediante el reconocimiento de su trayecto anatómico, ya que se ubica generalmente lateral a la línea media aproximadamente a 6- cm a nivel de la sínfisis del pubis cm a nivel umbilical a de la apófisis ioides.
Pinzas y otros
Se han desarrollado diferentes instrumentos laparoscópicos como pinzas de tejido (disectores, sujetadores o “graspers”), tijeras, portaagujas, bajador de nudos, bolsas laparoscópicas, dispositivos de irrigación y succión, engrapadoras, “clips” y dispositivos de energía quirúrgica. (1-3) La presión intraabdominal normal comprende un rango de 0-6.5mmHg. Actualmente se recomienda seleccionar la presión más baja posible que permita un adecuado campo de visión (entre 8-12mmHg en pacientes no obesos) e iniciar la insuación a uos baos Lmin. Acceso inicial a la cavidad abdominal (10,11,12)
Las pinas de teido se pueden clasificar como traumáticas y a traumáticas, por ejemplo:
• Disector con o punta “Maryland”: roma, con traumática frecuencia utilizada en trócar de trabajo principal.
• Sujetador útil o “Grasper”: atraumático, para la tracción de los tejidos. (1,2)
Neumoperitoneo (7,8,9)
Propiedades ideales para elección del gas:
• Escasa absorción peritoneal
• Eectos fisioló icos reducidos
• Excreción rápida
• Incombustible
• Solubilidad sanguínea
• Embolización intravascular con efectos mínimos.
Actualmente se utiliza el dióxido de carbono ya que reúne la mayoría de las características descritas previamente, sin embargo, no está exento de generar cambios fisioló icos a nivel de dierentes sistemas
• Respiratorio: acidosis respiratoria (hipercapnia), disminución de la complianza pulmonar y la capacidad vital, aumento de la presión intratorácica (compresión diafragmática).
• Cardiovascular: disminución del retorno venoso e índice cardíaco, aumento de la resistencia vascular periférica, compresión de la vena cava inferior, bradicardia, hipotensión, arritmias.
• Renal: tasa disminución de filtración de la glomerular.
La presión intraabdominal normal comprende un rango de 0-6.5mmHg. Actualmente se recomienda seleccionar la presión más baja posible que permita un adecuado campo de visión (entre 8-12mmHg en pacientes no obesos) e iniciar la insuación a uos baos Lmin.
Acceso inicial a la cavidad abdominal (10,11,12)
Se describen diferentes técnicas para realizar el neumoperitoneo. En esta revisión detallaremos las más utilizadas: técnica abierta y técnica cerrada.
Técnica abierta o Técnica de Hassan:
• Descrita en 1971 con el objetivo de disminuir el embolismo aseoso insuación preperitoneal y las posibles lesiones vasculares y viscerales.
• Se realiza una incisión a nivel supra, infra o transumbilical, se diseca por planos hasta observar el punto de fiación del ombli o a la fascia, se retrae esta con pinzas Kocher y posteriormente se colocan dos suturas a nivel de la fascia que permitirán levantar la misma. Después, se incide la fascia y se ingresa a la cavidad abdominal introduciendo un trócar atraumático de 10mm o de 5mm.
• Evitar realizar incisiones sobre cicatrices previas para evitar el contacto con posibles adherencias
Técnica cerrada o técnica de Veress:
• La aguja de Veress (ideada en 1932 por Janos Veres) se utiliza para crear el neumoperitoneo previo a la colocación de los demás trócares. Esta aguja canulada posee en su parte más distal un extremo biselado y una estructura linear atraumática en su interior adaptada a un resorte. A medida que se va atravesando el tejido, la porción interna atraumática sale de la aguja para evitar lesiones. (Figura 3)
• Al igual que la técnica abierta, este abordaje cerrado se realiza generalmente a nivel de la cicatriz umbilical o punto de Palmer.
• Punto de Palmer: ubicado a nivel del hipocondrio izquierdo, 3 5 aproximadamente cm por debajo de los arcos costales en la línea medio clavicular izquierda.
• Previo a la inserción, es recomendable el vaciamiento gástrico.
• Contraindicado en pacientes con cirugías gástricas o esplénicas previas, masas gástricas esplenomegalia o pancreáticas.
• La angulación de introducción de la aguja pueda variar desde 45° en paciente no obesos hasta 90° en pacientes obesos.
El límite apro imado de uo a través de un trócar de 10mm de diámetro es de 6.5 (+/- 0.5) l/min, mientras que el de una aguja de Veress es de 2.4l/min a 15mmHg.
Consideraciones técnicas generales
Al realizar un procedimiento laparoscópico existen diferencias con respecto a la cirugía abierta a considerar:
Visión (1,2,13)
• Al ingresar a la cavidad, se sugiere la realización de laparoscopía diagnóstica.
• La imagen proyectada es aproximadamente 16-20 veces mayor que la real. (2)
• Los sistemas de visión Clasicos reciben la imagen de la cavidad abdominal. la luz pasa a través de un prisma y es detectada por sensores tipo bastón para convertir la imagen óptica en digital a nivel del monitor, con una percepción en dos dimensiones
• Las últimas tecnologías en calidad de imagen emplean modalidades en tres dimensiones en alta definición Hi h Definition o ultraalta definición para optimi ar la eperiencia visual transoperatoria y crear la ilusión de profundidad (estereoscopía). La imagen es capturada desde la punta del laparoscopio y se transmite la señal eléctrica a un procesador. E iste una variedad si nificativa de diseos de sistemas de captura visual que generan diferencias en la calidad de la imagen percibida.
• Balance de blancos o “white balance”: el material blanco como las asas reean la lu y el material oscuro, como la sangre, absorbe luz. La opción de “balance de blancos” es una unción confi urable a nivel del cabezal de la cámara. Al enfocar un material color blanco y accionar esta opción, la camara recibe la referencia del “blanco verdadero” y mostrará correctamente el resto de los colores.
• Empañamiento del lente: cambios de temperatura del quirófano y el paciente que provocan condensación en la punta del lente. Algunos métodos para evitar esta situación incluyen: colocar el lente en agua caliente previo a su introducción a la cavidad abdominal, utilizar dispositivos para limpieza de lentes, o la salida de gas momentánea a través de un puerto secundario.
Instrumentos (2,3)
1. La utilización de instrumentos a distancia de los tejidos manipulados representa una limitante considerando los datos proporcionados por la háptica del cirujano.
2. Se recomienda accionar los dispositivos de energía y realizar las disecciones enfocando la punta del instrumento para evitar lesiones inadvertidas, así como retirar cualquier instrumento que no esté en uso.
Condiciones especiales
1. Obesidad: puede causar la migración de puntos anatómicos de referencia usuales y profundidad de la pared abdominal. Ingreso a cavidad se aborda con frecuencia con el uso de técnica cerrada. Se requieren instrumentos de mayor longitud. (2)
2. Embarazo: independientemente del trimestre, guías actuales apoyan su utilización en la resolución de apendicitis, patología biliar y resección de múltiples órganos sólidos. La posición del útero debe valorarse según la edad gestacional de la paciente. (2, 14)
3. Gerontes : los beneficios +son extrapolables a este grupo etario. (1,2)
Cierre (2)
1. Al finali ar el procedimiento se debe inspeccionar la cavidad por lesiones o sangrados inadvertidos.
2. El retiro de puertos debe realizarse a visión directa.
3. Cierre de fascia en puertos superiores a 5mm en diámetro y sitios de extracción de piezas con suturas continuas o interrumpidas.
Consideraciones posoperatorias (1,2)
1. La recuperación se asocia con posoperatoria menos dolor y días intrahospitalarios que la cirugía abierta.
2. El dolor severo es inusual. Ante duda significativa se debe considerar reintervención.
CONCLUSIONES
• Las múltiples ventajas observadas con la cirugía mínimamente invasiva han motivado al cirujano general a adoptar este tipo de procedimientos como la primera línea para la resolución de diferentes patologías de la cavidad abdominal.
Disminución de dolor posoperatorio, días intrahospitalarios y complicaciones figuran entre sus principales bondades.
• El cirujano se beneficia de meor visuali ación de estructuras con maor manificación.
• La vía de acceso de elección sigue siendo motivo de debate.
• El entendimiento del equipo, ergonomía y principales complicaciones es esencial para una laparoscopía segura.
• Se considera un abordaje seguro en la mayoría de grupos de pacientes, incluyendo embarazadas, pacientes bariátricos y geriátricos.
• Es una disciplina en constante evolución y constituye una plataforma para técnicas de más reciente introducción como la cirugía robótica.
REFERENCIAS BIBLIOGRÁFICAS
1. Levy, B., & Mobasheri, M. (2014). The principles of safe laparoscopic surgery. Surgery (Oxford), 32(3), 145-148.
2. Limb, C., & Rockall, T. (2020). Principles of laparoscopic surgery. Surgery (Oxford), 38(3), 161-171.
3. Chauvet, P., Rabischong, B., Curinier, S., Gremeau, A. S., Bourdel, N., Kaemmerlen, A. G., et al. (2018). Laparoscopia y cirugía laparoscópica: principios generales e instrumental. EMC Ginecología-Obstetricia, 54(2), 1-17.
4. Richardson, W. S., Hamad, G. G., Stefanidis, D., & SAGES Guidelines Committee (2017). SAGES VTE prophylaxis for laparoscopic surgery guidelines: an update. Surgical endoscopy, 31(2), 501–503.
5. Pouliquen, X. (2009). Técnicas básicas en cirugía laparoscópica del adulto. EMC-Técnicas Quirúrgicas-Aparato Digestivo, 25(2), 1-26.
6. Bouré L. (2005). General principles of laparoscopy. The Veterinary clinics of North America. Food animal practice, 21(1), 227–249.
7. Neudecker, J., Sauerland, S., Neugebauer, E., Bergamaschi, R., Bonjer, H. J., Cuschieri, A., et al. (2002). The European Association for Endoscopic Surgery clinical practice guideline on the pneumoperitoneum for laparoscopic surgery. Surgical endoscopy, 16(7), 1121–1143.
8. Merlin, T. L., Hiller, J. E., Maddern, G. J., Jamieson, G. G., Brown, A. R., & Kolbe, A. (2003). Systematic review of the safety and effectiveness of methods used to establish pneumoperitoneum in laparoscopic surgery. The British Journal of Surgery, 90(6), 668–679.)
9. Safran, D. B., & Orlando III, R. (1994). Physiologic effects of pneumoperitoneum. American Journal of Surgery, 167(2), 281-286.
10. Vilos, G. A., Ternamian, A., Dempster, J., Laberge, P. Y., & Clinical Practice Gynaecology Committee. (2007). Laparoscopic entry: a review of techniques, technologies, and complications. Journal of obstetrics and gynaecology Canada, 29(5), 433–447.
11. Ahmad, G., Baker, J., Finnerty, J., Phillips, K., & Watson, A. (2019). Laparoscopic entry techniques. The Cochrane database of systematic reviews, 1(1)
12. Hunter, J., Spight, D., Sandone, C., & Fairman, J. (2018). Altas of Minimally Invasive Surgical Operations (2nd Edition). New York: McGraw-Hill Education Illustrations.
13. Schwab, K., Smith, R., Brown, V., Whyte, M., & Jourdan, I. (2017). Evolution of stereoscopic imaging in surgery and recent advances. World journal of gastrointestinal endoscopy, 9(8), 368–377.
14. Pearl, J. P., Price, R. R., Tonkin, A. E., Richardson, W. S., & Stefanidis, D. (2017). SAGES guidelines for the use of laparoscopy during pregnancy. Surgical endoscopy, 31(10), 3767–3782
IDENTIFICACIÓN DE ORCID
Maria abriella Della Sera Lasso 0000-0002-6101-66
Marco Antonio Achurra Olmos 0009-0007-0044-9720
Víctor Bruno 0000-0003-0166-6974