Revista Médico Científica UNACHI
REVISIÓN LITERARIA
Eficacia del metotrexato, como monoterapia, en el tratamiento de la neutropenia en el Síndrome de Felty. Una revisión bibliográfica.
Effectiveness of methotrexate as monotherapy in the treatment of neutropenia in Felty's syndrome. A Literature review.
Autor:
Díaz García, Niko A.
Universidad de Panamá
Recibido: 4 de abril 2025; aceptado: 16 de mayo 2025
Disponible en internet: 31 de enero de 2025
PALABRAS CLAVES: Síndrome de Felty, Metotrexato, Neutrófilos, Artritis Reumatoide.
KEY WORDS: Bariatric Surgery, COVID-19, SARSCoV-2, Obesity, Weight Loss
RESUMEN
Introducción: El síndrome de Felty (SF) es un subtipo severo y raro de la artritis reumatoide (AR), con la tríada de esplenomegalia, neutropenia y artritis reumatoide. El metotrexato (MTX) es un antimetabolito del folato, que inhibe la dihidrofolato reductasa y la timidilato sintetasa, utilizado como primera línea en SF.
Objetivo: Evaluar la eficacia y seguridad del MTX en la neutropenia asociada al SF.
Materiales y métodos: Se realizó una revisión bibliográfica en PubMed, TRIP database, ClinicalTrials.gov, Cochrane y SciELO. De 114 artículos identificados, se incluyeron 7 estudios con un total de 11 pacientes diagnosticados con SF. Se analizó el efecto del MTX sobre el conteo absoluto de neutrófilos.
Resultados: Se analizaron 11 casos clínicos, de los cuales todos mostraron una mejoría clínica y estadísticamente significativa (p<0.01) del conteo absoluto de neutrófilos, con un promedio de 2,763.9 ± 1,629.6 células/ mm³; Adicionalmente, el 91% de los pacientes mostraron una mejoría articular y reducción de la velocidad de eritro sedimentación (VES), con una reducción promedio de 41.29 mm/h ± 29.68 mm/h. Ningún paciente presentó un efecto adverso que indicara el reemplazo de la terapia, solo dos tuvieron una erupción cutánea y síntomas gastrointestinales leves
Conclusión: El metrotexato como monoterapia es una opción segura y eficaz en el manejo del síndrome de Felty, con beneficios importantes en los neutrófilos, reducción de infecciones y manejo de artritis reumatoide de base. Sin embargo, se necesitan estudios amplios y controlados para confirmar estos hallazgos.
ABSTRACT
Introduction: Felty’s syndrome (FS) is a rare and severe subtype of rheumatoid arthritis (RA), characterized by the triad of splenomegaly, neutropenia, and RA. Methotrexate (MTX), a folate antagonist that inhibits dihydrofolate reductase and thymidylate synthase, is considered first-line therapy in FS.
Materials and Methods: A literature review was conducted using PubMed, TRIP database, ClinicalTrials.gov, Cochrane, and SciELO. From 114 identified articles, 7 studies were included, analyzing a total of 11 patients diagnosed with FS were included. The effect of MTX on absolute neutrophil count was analyzed.
Results: 11 clinical cases were analyzed, of which all showed a clinical and statistically significant (p<0.01) improvement in absolute neutrophil count, with an average of 2,763.9± 1,629.6 cells/ mm³; Additionally, 91% of the patients showed joint improvement and reduction of erythrocyte sedimentation rate (ESR), with an average reduction of 41.29 mm/h ± 29.68 mm/h. No patient had an adverse effect indicating therapy replacement, only two had a skin rash and mild gastrointestinal symptoms.
Conclusion: Methotrexate as monotherapy is a safe and effective treatment option for FS, improving neutrophil counts, reducing infection risk, and managing underlying RA symptoms. However, larger and controlled studies are necessary to confirm these findings.
INTRODUCCIÓN
El Síndrome de Felty (SF) es un subtipo severo, poco común de AR, presente en <1% de los pacientes, de los cuales el 60-80% son mujeres 1. Descrito por Augustus Roi Felty en 1924 con la tríada de: Esplenomegalia, conteo absoluto de neutrófilos (CAN) <2000/microL y AR. Esta disminución en los neutrófilos causa un aumento considerable en la tasa de infecciones y complicaciones relacionadas con la AR. 2 Las infecciones de piel y tracto respiratorio son las más comunes; debido en su mayoría por úlceras en la piel, terapia con glucocorticoides, severidad de la propia enfermedad y CAN <1000 células/microL. 3.
La presencia de neoplasias, específicamente de linfoma no Hogdkin es más común en los pacientes con SF con respecto a la población con AR y la general. También existe un aumento notorio de los síntomas extraarticulares como: úlceras en las piernas y vasculitis.4. Adicionalmente, a la neutropenia, puede coexistir una anemia de enfermedades crónicas y una trombocitopenia debido al secuestro esplénico y una médula ósea hiperplásica5.
Desde hace varios años, los fármacos antirreumáticos modificadores de la enfermedad (FARME) constituyen el pilar del tratamiento estándar en pacientes con artritis reumatoide (AR). Dentro de este grupo, el metotrexato (MTX) es considerado el fármaco de elección en pacientes con síndrome de Felty (SF), según múltiples reportes de casos 6,8. y consensos de expertos. Debido a la baja prevalencia del SF, no existen ensayos clínicos controlados, ni a gran ni a pequeña escala, que orienten su manejo. Tampoco existen guías terapéuticas específicas emitidas por el American College of Rheumatology (ACR) o la European League Against Rheumatism (EULAR), fundamentalmente por la rareza de esta entidad. En consecuencia, el tratamiento se extrapola del abordaje de la AR, ya que el SF se considera una manifestación extraarticular grave de esta enfermedad.
El objetivo de tratamiento se basa en buscar: a) Cambio en el CAN >2000 células/microL más dos de estas: b) Disminución de las infecciones % c) Disminución de las úlceras cutáneas d) Disminución de los episodios febriles.9.
El mecanismo de acción del MTX, en el contexto de la AR, es que libera adenosina que tiene función antiinflamatoria, afecta a la translocación del factor nuclear-κB al núcleo, a la señalización a través de la vía Janus quinasa y a la producción de óxido nítrico.10,12.
Los síntomas adversos más comunes al uso del MTX en dosis bajas (7,5 mg a 25 mg), son náuseas 13, erupción cutánea, neurotoxicidad 5.9% 14, hepatotoxicidad 5 %; 15 y toxicidad pulmonar con una incidencia del 1 al 5%.16,18
Con base en una necesidad de evaluar, de forma actualizada y resumida, las distintas fuentes bibliográficas, realizamos esta revisión de literatura para conocer la respuesta del MTX en los pacientes con SF y el cambio en los neutrófilos.
MATERIAL Y MÉTODOS
Fuentes de base de datos
Se llevó a cabo una búsqueda a través de: PubMed, TRIP database, ClinicalTrials.gov, Cochrane y SciELO. Se utilizó: “Felty syndrome” AND “Methotrexate” y “Felty syndrome” AND “Methotrexate” AND “Neutrophilia”. No hubo restricción de año, se utilizaron todos los artículos hasta el 12 de diciembre de 2024. No hubo restricción geográfica.
Criterios de inclusión de artículos
Los criterios son:
a) artículos completos en inglés y español
b) Reporte de casos, metaanálisis, ensayos controlados aleatorizados, revisiones, ensayos clínicos y revisiones sistemáticas.
Tipos de participantes
Los criterios son:
a) Adultos > 18 años
b) Con diagnóstico de síndrome de Felty:
1. neutropenia por laboratorio: <2000/microL; 2. esplenomegalia: por USG, CAT o examen físico; 3. Criterios de AR según: 2010 American College of Rheumatology (ACR) /European League Against Rheumatism (EULAR)19.
Exclusión: pacientes con un conteo absoluto de neutrófilos mayor a 2000 células/microL, pacientes con causas alternas de neutropenia, si utilizan concomitantemente; rituximab, hidroxicloroquina, sulfasalazina, leflunomida, tofacitinib, adalimumab, infliximab, etanercept, baricitinib, antecedentes personales patológicos de: enfermedades cardíacas, cirrosis, enfermedad renal crónica, embarazadas o alergia al MTX previo al diagnóstico.
Tipo de intervención
Utilizaron MTX a dosis bajas; desde 7,25 mg hasta 25 mg semanal vía oral, intramuscular (IM) o subcutáneo (SC).
Resultado primario
- Cambio en el recuento absoluto de neutrófilos.
Resultados secundarios
- Mejoría de los síntomas de la artritis reumatoide (sinovitis, artritis).
- Reducción de la tasa de infecciones.
- Tolerancia general al metotrexato.
- Mejoría en valor del VES.
Selección de estudios
Se llevó a cabo la búsqueda en las bases de datos previamente mencionadas, luego el autor revisó el título y resumen de resultados. Posteriormente, realizó la revisión del texto completo.
LOS RESULTADOS
Búsqueda de literatura
Se efectuó una búsqueda a través de: PubMed (n=39), TRIP database (n=59) ClinicalTrials.gov (n=0) y Cochrane (n=7) y SciELO (n=9). Se excluyeron: 2 artículos por ser < 18 años, 6 por utilizar hidroxicloroquina, 18 por utilizar rituximab, 7 por utilizar etanercept, 5 por utilizar leflunomida, 3 por adalimumab, 2 por no tener esplenomegalia, 6 por el CAN > 2000, 1 por no utilizar FARME. Ver figura 1.
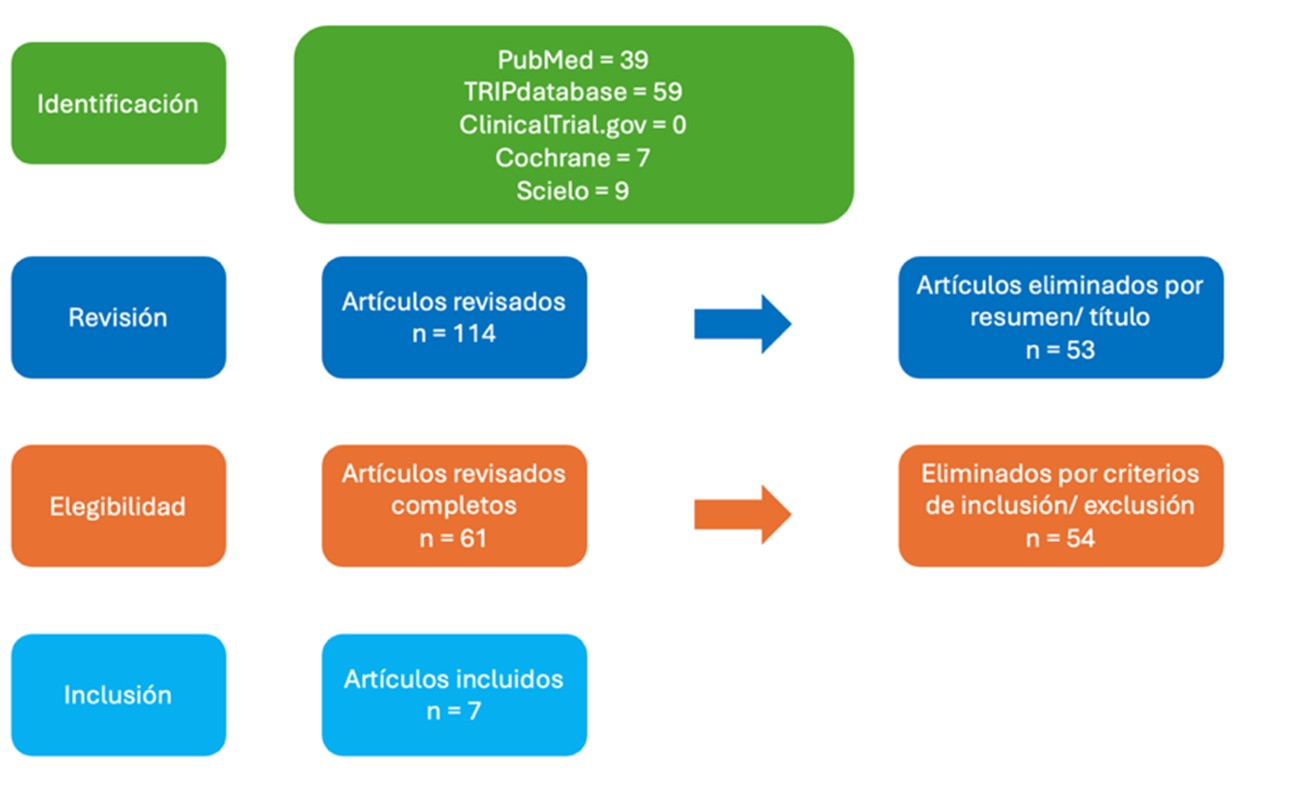
Caracteristicas generales del estudio
Los diseños incluidos fueron: a) Reporte de casos (n=6), metaanálisis (n=0), estudio observacional retrospectivo (n=1), ensayos clínicos controlados aleatorizados (n=0), revisiones (n=0), y revisiones sistemáticas (n= 0). Ver tabla 1.
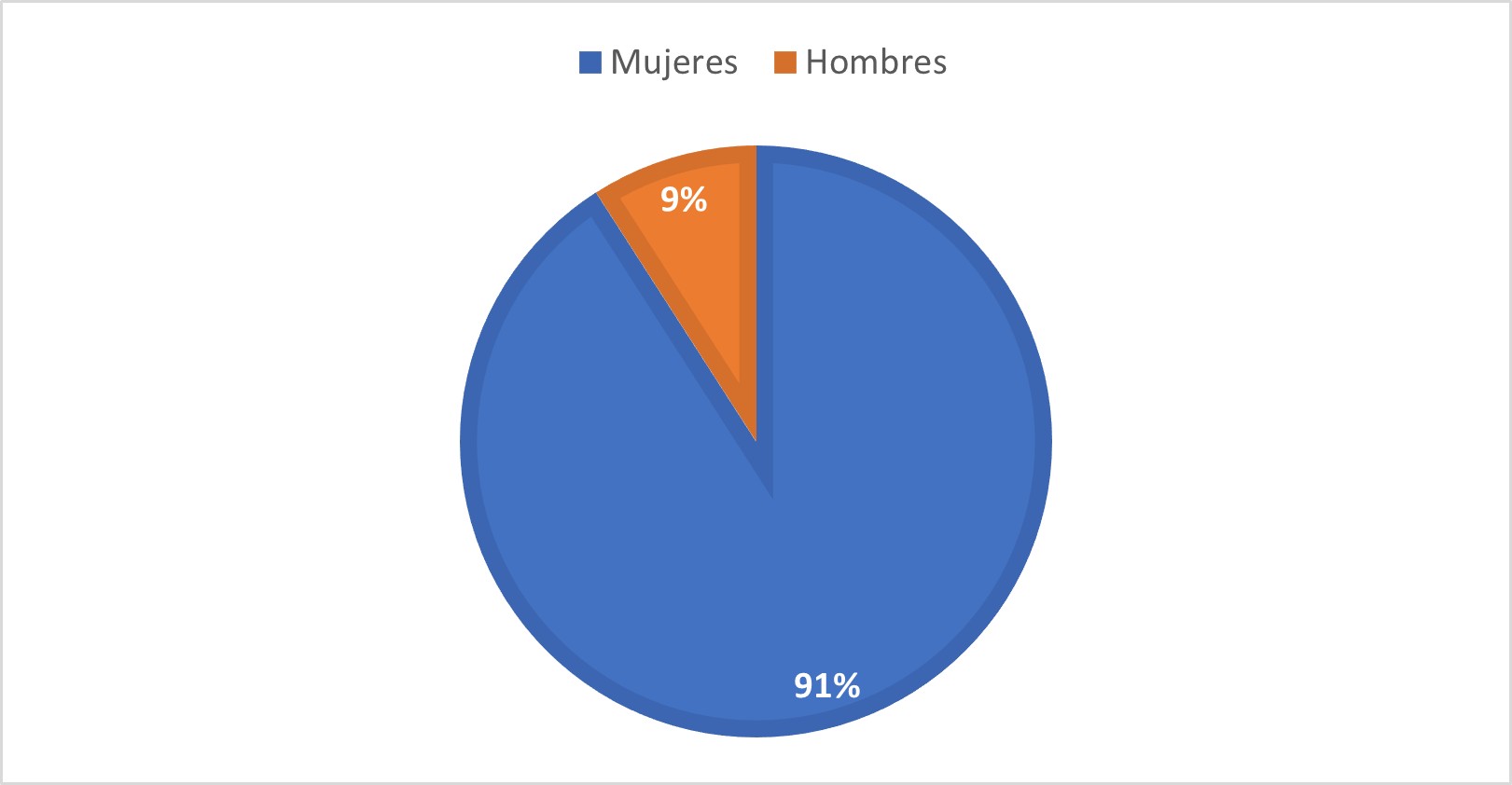
Los sitios demográficos de los pacientes reportados fueron: 3 de Estados Unidos 7,,20,21, Alemania22, 1 Bolivia 23, 1 Brasil24 y 1 China 25. Todos en un ambiente hospitalario.
Con respecto al metrotexato, todos fueron administrados vía oral, con una media 9,77 mg/semana. Una relación 10:1 en cuanto a la relación mujeres, hombres se refiere. (Ver gráfico 1).
| Autor y año | Edad y sexo | Dosificación | Seguimiento desde el inicio del tratamiento | Resultados primarios (CAN inicial a CAN final) | Resultados secundarios |
|---|---|---|---|---|---|
| Allen L 1986 7 | M 70 | 6,25 mg VO/semana | 30 meses | Aumento en el CAN:0 a 2,500 | Disminución de artralgias en 6 meses; disminución del VES y PCR (no cuantificado). Curación de úlceras de vasculitis en 9 meses. 1 hospitalización posterior con úlcera por presión sacra y del pie. |
| Fiechtner J 1989 20 *** | M 57 | 7,25 mg VO/semana | 10 meses | Aumento en el CAN: 1,900 a 6,000 | Articulaciones afectadas: 36 a 2; VES: 62 a 23; sin infecciones |
| Fiechtner J 1989 20 *** | M 50 | 7,25 mg VO/semana | 15 meses | Aumento en el CAN: 1,800 a 3,900 | Hubo empeoramiento parcial de rigidez articular y sinovitis en mano, muñeca, rodilla y pie; sin infecciones |
| Wassenberg S ** 1998 22 | M 46 | Media: 12,86 mg/semana | 12 meses | Aumento en el CAN: 1,960 a 3,360 | Articulaciones: 21 a 22; VES: 50 a 13; sin infecciones |
| Wassenberg S ** 1998 22 | M 61 | Media: 12,86 mg/semana | 12 meses | Aumento en el CAN: 1,276 a 3,557 | Articulaciones: 23 a 21; VES: 78 a 36; sin infecciones |
| Wassenberg S ** 1998 22 | M 62 | Media: 12,86 mg/semana | 12 meses | Aumento en el CAN: 462 a 4,977 | Articulaciones: 17 a 0; VES: 29 a 6; sin infecciones |
| Wassenberg S ** 1998 22 | M 55 | Media: 12,86 mg/semana | 12 meses | Aumento en el CAN: 1,936 a 2,172 | Articulaciones: 24 a 0; VES: 53 a 50; sin infecciones |
| Arando A 2015 23 | M 46 | - | - | Evolución favorable | |
| Amaral J 2018 24 | M 55 | 15 mg VO/semana | 5 meses | Aumento en el CAN: 414 a 4,368 | DAS28: 7.3 a 2.2; VES: 65 a 20; CDAI: 72 a 2.0; sin infecciones |
| Nimri D 2019 21 | M 64 | No se menciona | 2 semanas | Aumento en el CAN: 387 a 1,530 | VES: 78; PCR: 238.8; Evolución favorable en la sintomatología articular. |
| Yueming L 2024 25 | H 65 | 10 mg VO/semana | 2 meses | Aumento en el CAN: 490* a 5,900 | DAS28: 5.4 a 3.2; VES: 112 a 12; PCR: 99 a <8; 1 infección pulmonar por COVID-19 y colitis |
*Valor más bajo. **Tres pacientes tenían un CAN mayor a 2000 células/mm³ al momento del inicio del tratamiento, por lo que fueron excluidos. ***No se incluyeron los pacientes 1 y 2 debido a que no presentaban esplenomegalia.
Resultados primarios
En los 11 casos presentados hubo un aumento considerable y clínicamente relevante del CAN, lo que presenta una tendencia clara y consistente en la respuesta al tratamiento. Con un promedio de 2,763.9± 1,629.6 células/ mm³; (p<0.01). Ver resultados en Tabla 1.
Resultados secundarios
Mejoría de los síntomas de la artritis Reumatoide
En el 91% de los pacientes se observó una mejoría en la sintomatología de AR: la rigidez matutina > 60 minutos, artritis, artralgias y manifestaciones extraarticulares clásicas (nódulos reumatoideos, vasculitis, etc.). Y los dos pacientes que evaluaron el DAS28 presentaron una reducción superior a 1,2 21,25 que se traduce en una especificidad del 80 % que haya habido en una mejora del estado artritis.26
Reducción de la tasa de infecciones
De los 11 pacientes evaluados, uno tuvo una hospitalización tras el inicio del tratamiento con MTX, presentando complicaciones de úlceras por presión en la región sacra y el pie.7 En Yueming L, un paciente presentó un cuadro de colitis con diarrea y una infección pulmonar por COVID-19, para lo cual recibió tratamiento sintomático y molnupiravir 0.8 g cada 12 horas durante 5 días, respectivamente. Respondiendo favorablemente, con mejoría de la fatiga y la temperatura corporal.25
Tolerancia general al metrotexato/ Efectos adversos
El MTX en dosis bajas es altamente tolerable y prácticamente no presenta efectos adversos. Un paciente presentó un efecto adverso leve, probablemente asociado a una dosis de 7.5 mg/semana. Ante la aparición de síntomas gastrointestinales leves (náuseas y vómitos), la dosis se ajustó a 7.5 mg cada 10 días, lo que llevó a una resolución inmediata y completa de los síntomas. 20 Similarmente, otro paciente desarrolló una erupción cutánea con una dosis de 12.5 mg/semana, con base en la sospecha de que sea un efecto adverso al medicamento. Se redujo la dosis a 7.5 mg/semana, lo que dio como resultado la resolución completa de los síntomas.20 (Ver gráfica 2)
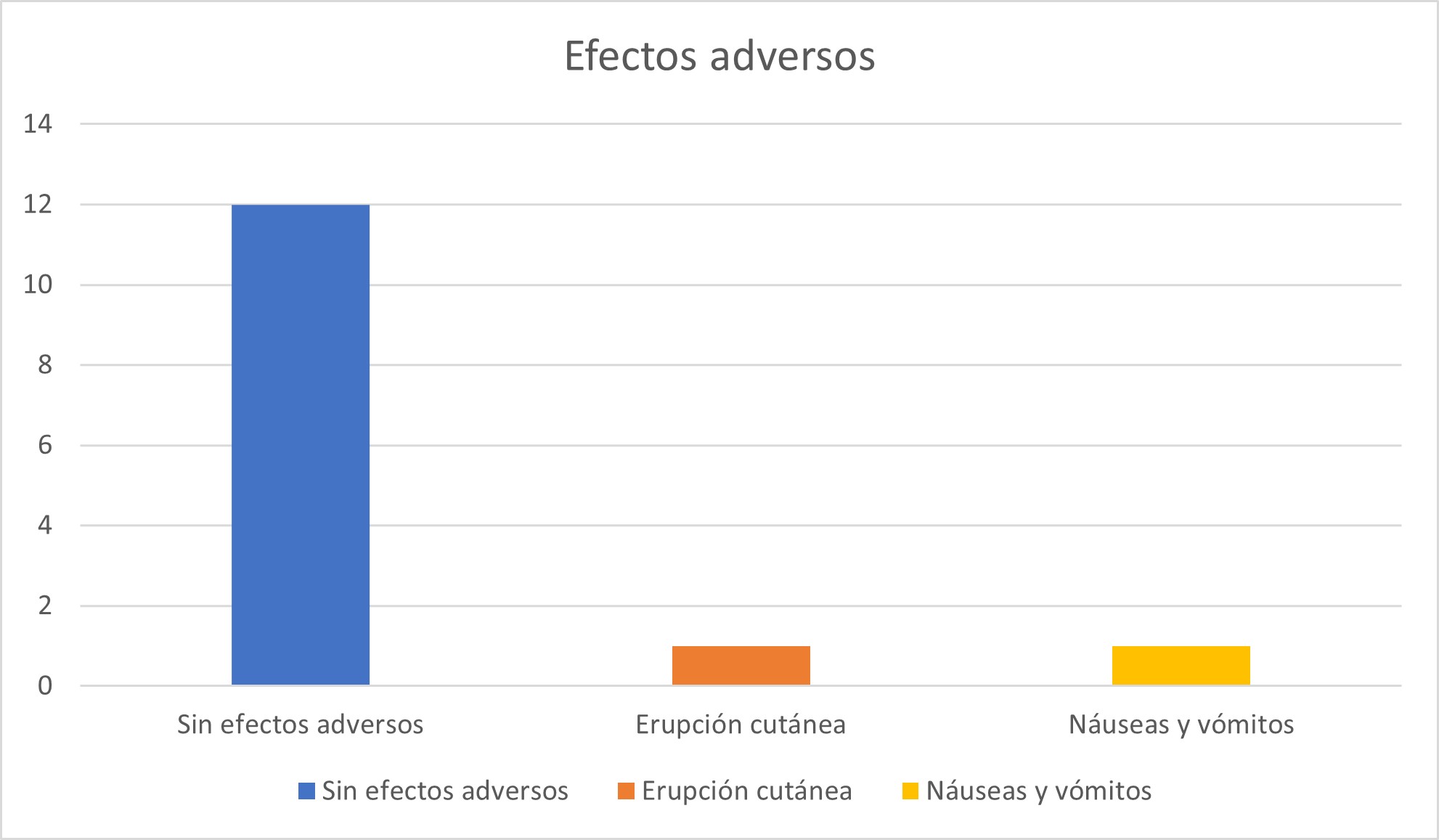
Evaluando el VES
El VES, un reactante inflamatorio importante en la AR, presentó una tendencia importante a la reducción con un promedio de: 41.29 mm/h ± 29.68 mm/h.
DISCUSIÓN
El objetivo de este estudio fue identificar, con la evidencia disponible, la seguridad y eficacia del MTX en la regulación del CAN, utilizando los casos clínicos dispuestos en la literatura. De manera general, los casos se reportaron de manera no sistemática y hacía falta información relevante en algunos casos.23
Se refuerza la eficacia del MTX como primera línea en el tratamiento del SF2, clínica y hubo estadísticamente, se demostró una mejoría significativa en el CAN con un aumento promedio de 2,763.9± 1,629.6 células/ mm³; (p<0.01). Adicionalmente, el MTX mostró una eficacia global en el manejo de la AR de base, ya que el 91% de los pacientes respondieron de manera positiva al tratamiento. Y los pacientes que evaluaron el puntaje DAS28, tuvieron una mejoría > 1.2, que se traduce como una reducción significativa de los síntomas de artritis. 27
El MTX presenta síntomas adversos comunes, como las náuseas, nefrotoxicidad, hepatotoxicidad, estomatitis, toxicidad pulmonar, entre otros. 28 En los 11 pacientes analizados, no se reportó ningún síntoma severo al tratamiento con dosis bajas que significara un cambio en la medicación. La erupción cutánea y síntomas gastrointestinales no son indicativos de esto. Solo un paciente se complicó con una infección pulmonar por COVID-19, pero respondió prontamente a la terapia de molnupiravir y no falleció.25
También hubo una reducción clínica importante del VES del: 41.29 mm/h ± 29.68 mm/h que se traduce como un marcador positivo en la disminución de la inflamación sistémica y la actividad de la enfermedad29.
La principal limitación del estudio es que todos los datos provienen de reportes de casos y estudios observacionales, debido a que no existen ensayos clínicos aleatorizados, principalmente por la rareza de la enfermedad, lo cual introduce un sesgo de selección y publicación. Adicional a esto, generó una barrera importante para poder generar resultados y análisis estadísticos de manera profunda, adicionalmente, no existe una forma sistemática de reportar datos y la mayoría de los pacientes tuvieron un seguimiento corto, creando una heterogeneidad importante, reduciendo la validez interna y externa.
Dada la evidencia actual, es fundamental llevar a cabo estudios más amplios, sistemáticos y controlados que confirmen la eficacia y seguridad del MTX en el tratamiento del SF. Aunque el MTX se posiciona como el tratamiento de elección en el SF, es relevante discutir otras opciones terapéuticas como; rituximab o hidroxicloroquina, que pueden ser utilizadas en casos refractarios al MTX. Futuras investigaciones podrían explorar el uso secuencial de MTX en conjunto con otros agentes.
Propongo que los siguientes reportes de casos del síndrome de Felty sean reportados de manera sistemática utilizando el CARE (CAse REport) Checklist30. Incluyendo datos relevante como la edad de inicio de la AR, valores de neutrófilos/VES/PCR al inicio y al final del curso de hospitalización, criterios diagnósticos utilizados tanto para el SF y AR y un seguimiento más prolongado de los pacientes; evaluando recaídas en las manifestaciones clínicas y tratamiento farmacológico, previo, durante y posterior a la presentación del SF, con dosis, vía de administración y duración.
CONCLUSIÓN
El metotrexato como monoterapia demostró ser una opción terapéutica eficaz y segura en el tratamiento de la neutropenia asociada al SF, mostrando una mejoría significativa en el conteo absoluto de neutrófilos y en la sintomatología de la artritis reumatoide de base. La mayoría de los pacientes presentaron una respuesta clínica favorable, con mínima incidencia de efectos adversos leves y buena tolerancia general al tratamiento. Sin embargo, debido a la limitada calidad metodológica y heterogeneidad de los estudios incluidos, los hallazgos deben interpretarse con cautela. Se destaca la necesidad urgente de estudios más amplios, sistemáticos y controlados que permitan validar de forma sólida la eficacia y seguridad del metotrexato en esta población específica.
IDENTIFICACIÓN ORCID:
- Niko A. Díaz García: 0009-0008-5618-030X
Referencias bibliográficas
1.Balint G. Felty’s syndrome. Best Practice & Research Clinical Rheumatology. 2004 Oct;18(5):631–45.
2.Wegscheider C, Ferincz V, Schöls K, Maieron A. Felty’s syndrome. Front Med (Lausanne) [Internet]. 2023;10. Disponible en: http://dx.doi.org/10.3389/fmed.2023.1238405
3.Breedveld FC, Fibbe WE, Hermans J, van der Meer JW, Cats A. Factors influencing the incidence of infections in Felty's syndrome. Arch Intern Med. 1987;147(5):915-920.
4.Gridley G, Klippel JH, Hoover RN, Fraumeni JF Jr. Incidence of cancer among men with the Felty syndrome. Ann Intern Med [Internet]. 1994;120(1):35–9. Disponible en: http://dx.doi.org/10.7326/0003-4819-120-1-199401010-00006
5.Hume R, Dagg JH, Fraser TN, Goldberg A. Anaemia of Felty’s syndrome. Ann Rheum Dis [Internet]. 1964;23(4):267–71. Disponible en: http://dx.doi.org/10.1136/ard.23.4.267
6.Isasi C, López-Martín JA, Angeles Trujillo M, Andreu JL, Palacio S, Mulero J. Felty's syndrome: response to low dose oral methotrexate. J Rheumatol. 1989;16(7):983-5.
7.Allen LS, Groff G. Treatment of Felty’s syndrome with low-dose oral methotrexate. Arthritis Rheum [Internet]. 1986;29(7):902–5. Disponible en: http://dx.doi.org/10.1002/art.1780290713
8.Verhoeven F, Guillot X, Prati C, Wendling D. Treatment of pseudo Felty’s syndrome: Is there a place for rituximab? Joint Bone Spine [Internet]. 2015;82(3):196–9. Disponible en: http://dx.doi.org/10.1016/j.jbspin.2014.12.001
9.Dillon AM, Luthra HS, Conn DL, Ferguson RH. Parenteral gold therapy in the Felty syndrome. Medicine (Baltimore). 1986;65(2):107-12.doi:10.1097/00005792-19860300000003 .
10. Cronstein BN, Aune TM. Methotrexate and its mechanisms of action in inflammatory arthritis. Nat Rev Rheumatol. 2020;16(3):145-54. doi: 10.1038/s41584-020-0373-9 .
11. Zhao Z, Hua Z, Luo X, et al. Application and pharmacological mechanism of methotrexate in rheumatoid arthritis. Biomed Pharmacother. 2022; 150:113074. doi: 10.1016/j.biopha.2022.113074 .
12. Katturajan R, S V, Rasool M, Evan Prince S. Molecular toxicity of methotrexate in rheumatoid arthritis treatment: a novel perspective and therapeutic implications. Toxicology. 2021;461:152909. doi: 10.1016/j.tox.2021.152909.
12. Katturajan R, S V, Rasool M, Evan Prince S. Molecular toxicity of methotrexate in rheumatoid arthritis treatment: a novel perspective and therapeutic implications. Toxicology. 2021;461:152909. doi:10.1016/j.tox.2021.152909 .
14. Van Lint JA, Bakker T, Ten Klooster PM, van Puijenbroek EP, Vonkeman HE, Jessurun NT. Neuropsychiatric adverse drug reactions associated with low dose methotrexate in rheumatoid arthritis patients. Expert Opin Drug Saf [Internet]. 2022;21(3):417–23. Disponible en: http://dx.doi.org/10.1080/14740338.2022.2003328
15. Whiting-O'Keefe QE, Fye KH, Sack KD. Methotrexate and histologic hepatic abnormalities: a meta-analysis. Am J Med. 1991;90(6):711-6.
16. Conaghan PG, Quinn DI, Brooks PM, Day RO. Hazards of low dose methotrexate. Aust N Z J Med [Internet]. 1995;25(6):670–3. Disponible en: http://dx.doi.org/10.1111/j.1445-5994.1995.tb02851.x
17. Pang Z, Wang G, Ran N, et al. Inhibitory effect of methotrexate on rheumatoid arthritis inflammation and comprehensive metabolomics analysis using ultra-performance liquid chromatography-quadrupole time of flight-mass spectrometry (UPLC-Q/TOF-MS). Int J Mol Sci. 2018;19(10):E2894. doi: 10.3390/ijms19102894.
18. Sparks JA, Dellaripa PF, Glynn RJ, Paynter NP, Xu C, Ridker PM, et al. Pulmonary adverse events in patients receiving low‐dose methotrexate in the randomized, double‐blind, placebo‐controlled Cardiovascular Inflammation Reduction Trial. Arthritis Rheumatol [Internet]. 2020;72(12):2065–71. Disponible en: http://dx.doi.org/10.1002/art.41452
19. Aletaha D, Neogi T, Silman AJ, Funovits J, Felson DT, Bingham CO, et al. 2010 Rheumatoid arthritis classification criteria: An American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010;62(9):2569–81.
20. Fiechtner JJ, Miller DR, Starkebaum G. Reversal of neutropenia with methotrexate treatment in patients with Felty’s syndrome. Correlation of response with neutrophil-reactive IgG. Arthritis Rheum [Internet]. 1989;32(2):194–201. Disponible en: http://dx.doi.org/10.1002/anr.1780320212
21. Nimri D, Abdallah MA, Waqas QA, Abdalla A, Tantoush H. Severe neutropenia complicated with necrotizing fasciitis unveils a diagnosis of rheumatoid arthritis: A case report. Cureus [Internet]. 2019;11(2):e4079. Disponible en: http://dx.doi.org/10.7759/cureus.4079
22. Wassenberg S, Herborn G, Rau R. Methotrexate treatment in Felty’s syndrome. Rheumatology (Oxford) [Internet]. 1998;37(8):908–11. Disponible en: http://dx.doi.org/10.1093/rheumatology/37.8.908
23. Berrios Arando A, Mendoza Lopez Videla JN, Ramos Loza CM. Síndrome de Felty: reporte de caso. Rev Med La Paz [Internet]. 2015;21(2):46–9. Disponible en:http://www.scielo.org.bo/scielo.php?script=sci_arttext&pid=S1726-89582015000200007
24. Amaral JK, Schoen RT. A case report of chikungunya fever, rheumatoid arthritis, and Felty’s syndrome. Rheumatol Ther. 2018;5(1):293–301. doi:10.1007/s40744-018-0103-9 .
25. Li Y, Zhu F, Wen R, Hou T, Xie R, Qin J. The first case of Felty’s syndrome complicated by COVID-19 infection. J Inflamm Res. 2024;17:8853–60.
26. Ward MM, Guthrie LC, Alba MI. Clinically important changes in individual and composite measures of rheumatoid arthritis activity: thresholds applicable in clinical trials. Ann Rheum Dis. 2015;74(9):1691–6. doi:10.1136/annrheumdis-2013-205079 .
27. Solomon DH, Glynn RJ, Karlson EW, Lu F, Corrigan C, Colls J, et al. Adverse effects of low-dose methotrexate: A randomized trial. Ann Intern Med [Internet]. 2020;172(6):369. Disponible en: http://dx.doi.org/10.7326/m19-3369
28. Vanni KMM, Lyu H, Solomon DH. Cytopenias among patients with rheumatic diseases using methotrexate: a meta-analysis of randomized controlled clinical trials. Rheumatology (Oxford) [Internet]. 2020;59(4):709–17. Disponible en: http://dx.doi.org/10.1093/rheumatology/kez343
29. Abelson B, Sokka T, Pincus T. Declines in erythrocyte sedimentation rates in patients with rheumatoid arthritis over the second half of the 20th century. J Rheumatol [Internet]. 2009;36(8):1596–9. Disponible en: http://dx.doi.org/10.3899/jrheum.081255
30. Riley DS, Barber MS, Kienle GS, Aronson JK, von Schoen-Angerer T, Tugwell P, et al. CARE guidelines for case reports: explanation and elaboration document. J Clin Epidemiol [Internet]. 2017;89:218–35. Disponible en: http://dx.doi.org/10.1016/j.jclinepi.2017.04.026
